Durante más de 130 años los dinosaurios han sido clasificados en dos órdenes separados, los saurisquios y los ornitisquios. Pero como siempre pasa en las ciencias biológicas, toda teoría es cierta hasta que se demuestra lo contrario. Un nuevo estudio ha puesto en entredicho la clasificación clásica de los dinosaurios, eliminando y redistribuyendo algunos de los diferentes grupos de dinosaurios. Aunque esta nueva hipótesis no es segura al 100%, en esta entrada os explicaremos en que consiste este reordenamiento de los dinosaurios.
CLASIFICACIÓN TRADICIONAL DE LOS DINOSAURIOS
Desde el siglo XIX, los dinosaurios se han dividido en dos grandes órdenes basados en la estructura de su pelvis. El orden Saurischia (pelvis de lagarto) incluye a los terópodos (dinosaurios carnívoros y aves actuales) y a los sauropodomorfos (grandes herbívoros de cuello largo); el orden Ornithischia (pelvis de ave) incluye a los ornitópodos (dinosaurios herbívoros y con pico de pato), a los marginocéfalos (dinosaurios con cuernos y estructuras craneales reforzadas) y a los tireóforos (dinosaurios acorazados).
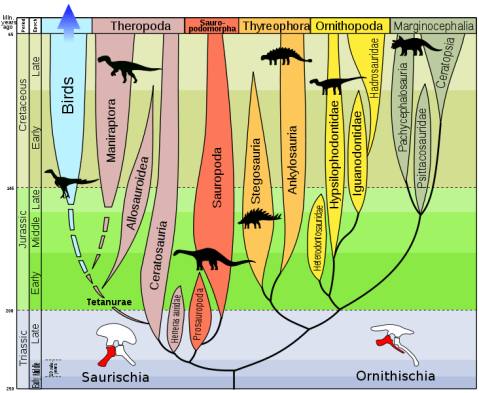
Aun así, esta clasificación no tiene la última palabra. La paleontología es una ciencia extremadamente volátil, ya que con cada nuevo descubrimiento se puede desmontar todo lo que se sabía hasta el momento, aunque se trate de una hipótesis centenaria. Esto es lo que ha pasado con los dinosaurios recientemente.
EL INICIO DE UNA NUEVA HIPÓTESIS
Un nuevo estudio publicado el marzo de 2017, ha hecho replantear la clasificación tradicional de los dinosaurios. Muchos estudios anteriores asumían como cierta la clasificación en Saurischia/Ornithischia tradicional y por lo tanto, los caracteres y los taxones utilizados ya iban enfocados a dicha clasificación. En cambio, este nuevo estudio ha sido pionero en varios aspectos:
- Incluye un gran número de especies y taxones (muchos más que en investigaciones anteriores).
- Estudios anteriores daban mucho más énfasis en dinosaurios terópodos y sauropodomorfos (saurisquios tradicionales) basales, ya que fueron de los primeros grupos en diversificarse, incluyendo pocos ornitisquios basales.
- También se han incluido muchos arcosaurios dinosauromorfos (taxones no dinosaurios).
- Estudios anteriores habían asumido que muchos caracteres de los ornitisquios eran simplesiomórficos (caracteres ancestrales de todos los dinosaurios) y sólo se centraban en pocas sinapomorfías (caracteres compartidos por un grupo monofilético).
Este estudio se ha desprendido de muchas de las suposiciones anteriores sobre filogenia dinosauria y ha analizado un gran número de especies y multitud de caracteres no incluidos en investigaciones anteriores. Esto ha hecho que el árbol evolutivo resultante fuese muy diferente de los que se habían obtenido hasta la fecha.
RECONSTRUYENDO EL ÁRBOL
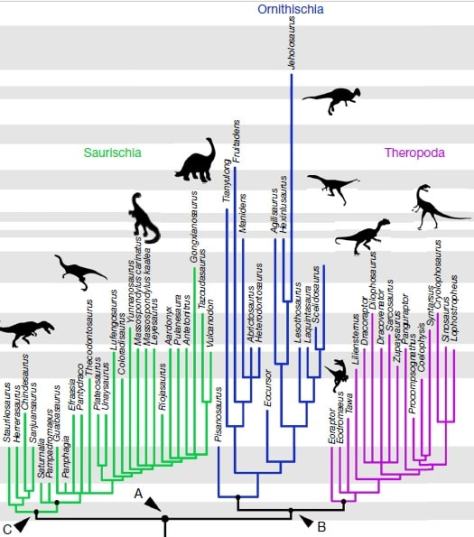
Entonces, ¿cómo queda el árbol evolutivo de los dinosaurios según esta hipótesis? Pues el tema es un poco complicado, aunque los diferentes taxones siguen quedando divididos en dos órdenes:
- El orden Saurischia que, según el estudio, sólo incluye a los sauropodomorfos y a los herrerasáuridos (grupo de saurisquios carnívoros no terópodos).
- El nuevo orden Ornithoscelida (patas de ave) que incluye a los ornitisquios tradicionales y a los terópodos, que dejan de ser saurisquios.
Teniendo esto en mente, veamos ahora las características que definen a estos dos grupos.
Saurisquios
El orden Saurischia se mantiene prácticamente igual, excepto que los terópodos quedan fuera del grupo. Este orden presenta la pelvis con estructura saurisquia original, como también la presentaban los antepasados de los dinosaurios. Según la nueva hipótesis, dentro de los saurisquios se incluyen los herrerasáuridos y los sauropodomorfos.
Los herrerasáuridos (familia Herrerasauridae) fueron un pequeño grupo de saurisquios basales que evolucionaron hacia una dieta carnívora. Por eso durante mucho tiempo se pensó que eran el grupo hermano de los terópodos, pero después se vio que su lugar se encontraba entre los primeros saurisquios. Aun estando bastante especializados, probablemente la competencia con otros depredadores hizo que no durasen mucho tiempo, apareciendo a mediados del Triásico y extinguiéndose a finales de este período.

Los herrerasáuridos ocupaban un nicho ecológico similar al de los terópodos. La nueva hipótesis implica entonces que la hipercarnivoría (alimentación exclusivamente de carne) evolucionó independientemente dos veces en los dinosaurios, cosa que hace que algunos paleontólogos la pongan en duda. Aun así, la anatomía de los herrerasáuridos y de los terópodos difería en ciertos aspectos, como la anatomía de sus manos (más generalista en los herrerasáuridos) y la estructura de la mandíbula.
Los primeros sauropodomorfos eran animales bípedos igual que los herrerasáuridos, aunque éstos eran animales omnívoros. Aun así, los sauropodomorfos acabarían convirtiéndose en enormes cuadrúpedos herbívoros con cuellos larguísimos característicos.

Ornitoscélidos
El nuevo orden de dinosaurios es Ornithoscelida, que agrupa los terópodos con los ornitisquios. Este taxón está apoyado por más de veinte sinapomorfías (caracteres derivados compartidos por un clado) esqueléticas, presentes tanto en terópodos como en ornitisquios basales. Algunas de estas características incluyen la presencia de una separación entre los dientes premaxilares y maxilares (diastema) y la fusión de los extremos de la tibia y la fíbula en un tibiotarso (aunque estos caracteres sólo se encuentran en las especies más basales).
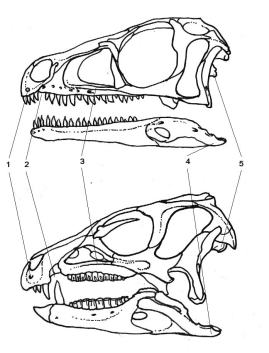
Tanto los terópodos como los primeros ornitisquios eran animales bípedos. Además, la presencia de dientes heterodontos en los miembros ancestrales de ambos grupos nos lleva a pensar que los primeros ornitoscélidos eran omnívoros, los cuáles después se especializarían en alimentarse de carne y de vegetación (terópodos y ornitisquios respectivamente).

Una curiosidad de la nueva clasificación es que aceptando a Ornithoscelida como un taxón válido, se agrupan a todos los dinosaurios con plumas en un solo grupo. Por todos es sabido que muchos terópodos presentaban plumas (ya que son los antepasados de las aves) pero, lo que mucha gente desconoce es que la presencia de plumas también se ha demostrado en algunos ornitisquios basales y en otros más avanzados.
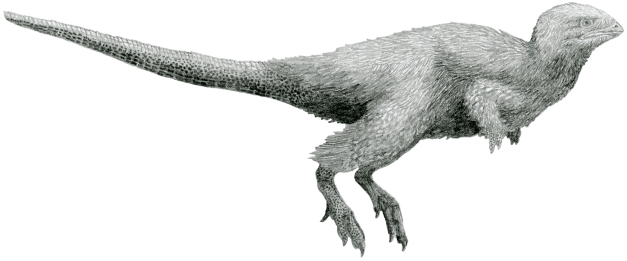
SEGUIR INVESTIGANDO
Y entonces, ¿es definitiva esta hipótesis? Pues no, por supuesto. Aunque resulta bastante atractivo decir que se ha cambiado la historia natural de los dinosaurios para siempre, no podemos asegurar que a partir de ahora los dinosaurios se clasifiquen de este modo.
Aunque este estudio muestre resultados interesantes sobre el origen de los dinosaurios, no se pueden ignorar los cientos de estudios anteriores que se han hecho sobre este grupo de animales. Deberemos estar atentos a nuevos artículos que poco a poco vayan desvelando más información sobre las relaciones entre estos reptiles mesozoicos. ¡Y es que esto es lo más estimulante de la biología, que no hay nada seguro! Y que con nuevas técnicas de estudio y nuevos descubrimientos, poco a poco aprendemos más sobre el mundo que nos rodea.
¡Mantened la mente abierta y seguid investigando!
REFERENCIAS
Se han consultado las siguientes fuentes durante la elaboración de esta entrada:
- G. Seeley (1887). On the Classification of the Fossil Animals Commonly Named Dinosauria. Proceedings of the Royal Society of London Vol. 43. Pp 165-171.
- Baron, Norman & Barret (2017). A new hypothesis of dinosaur relationships and early dinosaur evolution. Nature Vol. 543. Pp 501-506.
- Senter & Robins (2015). Resting Orientations of Dinosaur Scapulae and Forelimbs: A Numerical Analysis, with Implications for Reconstructions and Museum Mounts. Plos One.
- Scientific American. Ornithoscelida Rises: A New Family Tree for Dinosaurs.
- Imagen de portada de Charles Knight.