For more than 130 years dinosaurs have been classified into two distinct orders, the saurischians and the ornithischians. But as it is common in biological sciences, every theory is true until the opposite is proved. A new study has called into question classical dinosaur classification, destroying and redistributing some of the different dinosaur groups. Even if this new hypothesis isn’t 100% sure yet, in this entry we’ll explain what this dinosaur reordering consists in.
TRADITIONAL DINOSAUR CLASSIFICATION
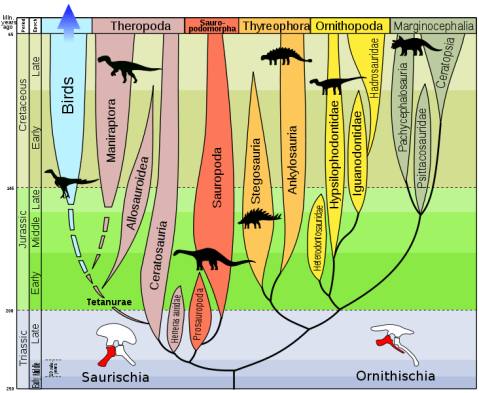
Since the XIX century, dinosaurs have been divided into two large orders based on their hip anatomy. The order Saurischia (lizard-hipped) includes theropods (carnivorous dinosaurs and current birds) and sauropodomorphs (large, long-necked herbivores); the order Ornithischia (bird-hipped) includes ornithopods (herbivorous and duck-billed dinosaurs), marginocephalians (dinosaurs with horns and hardened skulls) and thyreophorans (armored dinosaurs).
Yet, this classification doesn’t have the last word. Palaeontology is an extremely volatile science, as with each new discovery, you can dismantle everything you knew at that moment, even if it’s a centenary-old hypothesis. This is what has recently happened with dinosaurs.
THE RISE OF A NEW HYPOTHESIS
A new study published in March 2017, has caused the reconsideration of traditional dinosaur classification. Many previous studies assumed the Saurichia/Ornithischia classification as true and so, the used characters and taxons were all focussed on this classification. However, this new study has pioneered in many aspects:
- It includes a larger number of species and taxons (many more than in previous investigations).
- Previous studies gave more importance to basal theropod and sauropodomorph dinosaurs (traditional saurischians), as they were the first dinosaurs to diversify, including few basal ornithischians.
- It has also included many dinosauromorph archosaurs (non-dinosaur taxons).
- Older studies had assumed many ornithischian characters to be symplesiomorphies (ancestral characters of all dinosaurs) and they only focused on a few synapomorphies (characters found in a monophyletic group).
This study has detached from many of the previous assumptions on dinosaur phylogeny and has analysed a large number of species and many characters not included in previous investigations. This has made the resulting evolutionary tree pretty different from the ones obtained before.
RESHAPING THE TREE
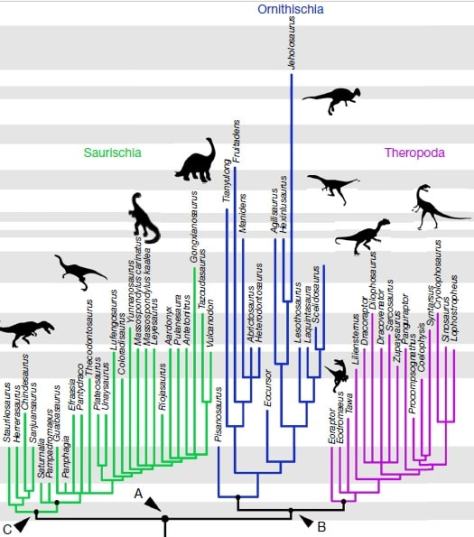
Then, how does the dinosaur’s evolutionary tree stand according to this hypothesis? Well, the matter is somewhat complex, even if the different groups are still divided in two orders:
- Order Saurischia which, according to this study, only includes sauropodomorphs and herrerasaurids (a group of carnivorous, non-theropod saurischians).
- The new order Ornithoscelida (bird-limbed) that includes the traditional ornithischians and theropods, which are no longer saurischians.
Keeping this in mind, let’s now see the characteristics that define these two orders.
Saurischians
The order Saurischia is almost the same, except that theropods are no longer part of this group. This order presents the original saurischian hip structure, which the dinosaurs’ ancestors also had. According to this new hypothesis, herrerasaurids and sauropodomorphs are all included as saurischians.
Herrerasaurids (Herrerasauridae family) were a small group of basal saurischians that evolved towards meat-eating. That’s why for a long time it was thought that they were the sister-taxon of theropods, but it was later seen that they were found among the first saurischians. Even if they were pretty specialized, they were probably displaced by competition with other predators, appearing during the middle Triassic and becoming extinct at the end of it.

Herrerasaurids occupied a similar ecological niche as theropods. The new hypothesis implies that hypercarnivory (feeding exclusively on meat) evolved independently twice in dinosaurs, which makes some palaeontologist question it. Yet the herrerasaurid and theropod anatomy differed in some aspects, such as the anatomy of their hands (more generalistic in herrerasaurids) and the jaw structure.
The first sauropodomorphs were biped animals just like herrerasaurids, even if they were omnivorous. Yet, sauropodomorphs would end up becoming huge herbivorous quadrupeds with characteristic long necks.

Ornithoscelidans
The new dinosaur order is Ornithoscelida, which groups theropods with ornithischians. This taxon is supported by more than twenty skeletal synapomorphies (derived characters shared by a clade), present both in basal theropods and ornithischians. Some of these characteristics include the presence of a gap between premaxillar and maxillar teeth (diastema) and the fusion of the ends of the tibia and the fibula into a tibiotarsus (even if these characteristics are only found on the most basal species).
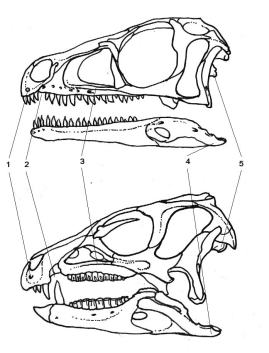
Both theropods and the first ornithischians were bipedal animals. Also, the presence of heterodont teeth in the ancestral members of both groups leads us to think that the first ornithoscelidans were omnivorous, which would later specialise in feeding on meat and on plants (theropods and ornithopods respectively).

A curiosity about the new classification is that accepting Ornithoscelida as a valid taxon, all feathered dinosaurs are put together into one group. Everyone knows that many theropods presented feathers (as they were the ancestors of birds) but, what most people don’t know is that feathers have also been found in some basal ornithischians and in more advanced ones too.
KEEP INVESTIGATING
Then, is this hypothesis irrevocable? Well, no of course. Even if it’s pretty tempting to assume that the dinosaur’s natural history has been changed, we cannot say that from now on dinosaurs will be classified this way.
Even if this study shows really interesting results about the origin of dinosaurs, we cannot dismiss hundreds of previous studies about this group of animals. We’ll have to remain alert to new articles that step by step will keep unveiling more information about the relationships between these Mesozoic reptiles. And that’s what’s so stimulating about biology, that there’s nothing sure! And that with new investigation techniques and new discoveries, little by little we learn more about the world around us.
Keep your mind open and keep investigating!
REFERENCES
The following sources have been consulted during the elaboration of this entry:
- G. Seeley (1887). On the Classification of the Fossil Animals Commonly Named Dinosauria. Proceedings of the Royal Society of London Vol. 43. Pp 165-171.
- Baron, Norman & Barret (2017). A new hypothesis of dinosaur relationships and early dinosaur evolution. Nature Vol. 543. Pp 501-506.
- Senter & Robins (2015). Resting Orientations of Dinosaur Scapulae and Forelimbs: A Numerical Analysis, with Implications for Reconstructions and Museum Mounts. Plos One.
- Scientific American. Ornithoscelida Rises: A New Family Tree for Dinosaurs.
- Cover image by Charles Knight.