Els mamífers van evolucionar dels rèptils? Doncs la veritat és que no. Rèptils i mamífers tenen històries evolutives independents que es van separar poc després de l’aparició de l’anomenat ou amniota, que permetia que les cries d’aquests animals nasquéssin fora de l’aigua. Anteriorment vam parlar sobre l’origen dels vertebrats, i sobre com aquests van sortir del mar per a caminar per terra per primer cop. En aquesta entrada explicarem com els avantpassats de rèptils i mamífers, els AMNIOTES, van independitzar-se del medi aquàtic i van convertir-se en el grup dominant d’animals terrestres.
L’OU AMNIOTA
La característica que uneix a rèptils i mamífers en un sol grup és l’ou amniota. Mentre que els ous dels amfibis són relativament petits i només presenten una capa interna, els ous dels amniotes són força més grans i presenten vàries membranes protegint l’embrió i mantenint-lo en un medi aquós. La capa més externa és la closca de l’ou, que apart d’oferir protección física a l’embrió, evita la pèrdua d’aigua i la seva porositat permet l’intercanvi de gasos. Sota la closca hi trobem les següents membranes:
Esquema de l’ou d’un cocodril: 1. closca de l’ou 2. sac vitel·lí 3. vitel (nutrients) 4. vasos sanguinis 5. amni 6. cori 7. aire 8. alantoide 9. albúmina (clara de l’ou) 10. sac amniòtic 11. embrió 12. líquid amniòtic. Imatge de Amelia P.
- Cori: És la primera membrana interna que trobem, proporciona protecció i, juntament amb l’amni, formen el sac amniòtic. A més, al estar en contacte amb la closca, participa en l’intercanvi de gasos, portant oxígen de l’exterior a l’embrió i diòxid de carboni de l’embrió a l’exterior.
- Amni: Membrana que envolta l’embrió i forma la part interna del sac amniòtic. Aquesta proporciona un ambient aquós a l’embrió, i el connecta amb el sac vitel·lí (estructura que proporciona aliment i que també es troba en peixos i amfibis).
- Alantoide: La tercera capa, serveix com a magatzem de residus nitrogenats, i juntament amb el cori ajuda en l’intercanvi de gasos.
Esquema de l’ou d’un amfibi: 1. càpsula gelatinosa 2. membrana vitel·lina 3. fluid perivitel·lí 4. vitel 5. embrió. Imatge de Separe3g.
Aquest seguit de membranes fan que els amniotes no hagin de tornar a l’aigua per a pondre els ous. A més, a diferència dels amfibis, els amniotes no passen per la fase larvària amb brànquies, sinó que neixen directament com a adults en miniatura, amb pulmons i potes (els que en tenen). Tot això va fer que els primers amniotes s’independitzéssin completament del medi aquàtic.
ORIGEN DELS AMNIOTES
Les primers amniotes van evolucionar fa uns 312 milions d’anys a partir de tetràpodes reptiliomorfs. A finals del Carbonífer van desaparèixer molts dels boscos tropicals on vivien els amfibis primitius, deixant lloc a un clima més fred i àrid. Això va acabar amb molts dels grans amfibis de l’época, deixant espai per a que els amniotes ocupéssin els nous hàbitats.
Reconstrucció de Solenodonsaurus janenschi, un dels candidats a ser el primer amniota, que visqué fa 320-305 milions d’anys a l’actual República Txeca. Recontrucció de Dmitry Bogdanov.
CARACTERÍSTIQUES
Aquests primers amniotes presentaven un seguit de característiques que els diferenciaven dels seus avantpassats semiaquàtics:
- Urpes còrnies (els amfibis no tenen urpes) i pell queratinitzada que redueix la pèrdua d’aigua.
- Intestí gruixut més gran i major densitat de túbuls renals, per augmentar la reabsorció d’aigua.
- Glàndules llacrimals especialitzades i una tercera membrana a l’ull (membrana nictitant) que mantenen la humitat ocular.
- Pulmons més grans.
- Pèrdua de la línia lateral (òrgan sensorial present en peixos i amfibis).
L’esquelet i la musculatura també van evolucionar oferint una major movilitat i agilitat en un hàbitat terrestre. Els primers amniotes presentaven les costelles tancades per davant mitjançant l’esternó, fent que els seus òrgans interns estiguéssin més ben subjectats, i un seguit de receptors musculars els conferien una major agilitat i coordinació durant la locomoció.
CRANIS AMNIOTES
Tradicionalment, es classificaven els diferents amniotes en base a l’estructura del seu crani. La característica que es mirava era la presència de obertures temporals (fenestres), segons les quals teníem tres grups:
- Anàpsids (“sense arcs”): No presenten cap obertura temporal (tortugues).
Esquema d’un crani anàpsid, de Preto(m).
- Sinàpsids (“arcs fusionats”): Presenten una sola obertura temporal inferior (mamífers).
Esquema d’un crani sinàpsid, de Preto(m).
- Diàpsids (“dos arcs”): Presenten dues obertures temporals (rèptils, incloent les aus).
Esquema d’un crani diàpsid, de Preto(m).
Abans es creia que els primers amniotes presentaven un crani anàpsid (sense obertures, com les tortugues) i que posteriorment es van separar els sinàpsids i els diàpsids (les obertures temporals formaven uns “arcs” que proporcionaren nous punts d’anclatge per la musculatura mandibular). Tanmateix, s’ha vist que aquesta classificació en tres grups no és vàlida.
Tot i que encara es creu que els primers amniotes eren anàpsids, actualment es pensa que aquests, molt poc després de la seva aparició, es van separar en dos llinatges diferents: els sinàpsids (clade Synapsida) i els sauròpsids (clade Sauropsida).
SYNAPSIDA
Aquest llinatge inclou als mamífers i als seus avantpassats amniotes. Tot i que els primers sinàpsids com Archaeothyris externament s’assemblessin a una sargantana, estaven més emparentats amb els mamífers i compartien amb aquests l’obertura temporal única per on passaven els músculs mandibulars.
Dibuix del crani de Archaeothyris, el que es creu que va ser un dels primers sinàpsids que visqué fa uns 306 milions d’anys a Nova Escòcia. Dibuix de Gretarsson.
Als avantpassats dels mamífers abans se’ls coneixia com a “rèptils mamiferoides”, ja que es creia que els mamífers havien evolucionat de rèptils primitius. Actualment és acceptat que els sinàpsids formen un llinatge independent dels rèptils, i que comparteixen un seguit de tendències evolutives que porten fins als mamífers moderns: l’aparició de diferents tipus de dents, la mandíbula formada per un únic os, la posició més vertical de les potes respecte el cos, etc…
Reconstrucció de Dimetrodon grandis, un dels sinàpsids més coneguts, de fa uns 280 milions d’anys. Reconstrucció de Dmitry Bogdanov.
Tot i que la majoria de mamífers actuals no pon ous i pareix a les cries vives, tots els grups durant el desenvolupament embrionari mantenen les tres membranes característiques dels amniotes (amni, cori i alantoide).
SAUROPSIDA
Els sauròpsids inclouen als rèptils actuals i als seus avantpassats i parents amniotes. Actualment en molts treballs científics s’utilitza la paraula “sauròpsid” en lloc de “rèptil” quan es discuteix de filogènia, ja que dins de sauròpsid s’inclou també a les aus. Els primers sauròpsids probablement eren anàpsids, i poc després de la seva aparició es van separar en dos grups: els Parareptilia que conservaven el crani anàpsid, i els Eureptilia que inclouen als diàpsids (els rèptils i aus actuals).
Arbre evolutiu dels vertebrats actuals, on es marca de color verd als grups antigament considerats rèptils. Com es veu, la concepció tradicional de “rèptil” inclou als avantpassats dels mamífers i exclou a les aus. Imatge de Petter Bøckman.
Els diàpsids actualment són el grup de vertebrats terrestres més diversificat. Aquests es van multiplicar en moltíssimes espècies a finals del Pèrmic (fa uns 254 milions d’anys), just abans del Mesozoic (l’Era dels Rèptils). Aquests es poden dividir en dos grans grups: els Lepidosaures i els Arcosaures, ambdós amb representants actuals.
LEPIDOSAURIA: PETITS I NOMBROSOS
Els lepidosaures (literalment “rèptils amb escates”) van aparèixer a principis del Triàssic (fa uns 247 milions d’anys) i, tot i que la majoria no van assolir grans mides, actualment són el grup de rèptils no aviaris més nombrós. Aquests es caracteritzen per presentar una escletxa cloacal transversal, per presentar escates sobreposades i mudar la pell sencera o a trossos i per altres caràcters esquelètics.
Muda sencera de la pell d’una serp rata. Foto de Mylittlefinger.
Els lepidosaures actuals pertanyen a dos ordres diferents:
- Ordre Rhynchocephalia: Inclouen a les dues espècies de tuatares actuals. Es consideren fòssils vivents perquè presenten cranis i característiques semblants a les dels diàpsids mesozoics i actualmente es troben en greu perill d’extinció.
Foto d’una tuatara (Sphenodon punctatus), de Tim Vickers.
- Ordre Squamata: Els escamosos actuals inclouen iguanes, camaleons, dragons, sargantanes, serps i altres llangardaixos sense potes. Amb més de 9000 espècies actuales els escamosos són un grup molt nombrós, amb un gran ventall d’adaptacions i estratègies de supervivencia.
Fotos d’alguns escamosos d’esquerra a dreta i de dalt a baix: Iguana verda (Iguana iguana, de Cary Bass), cobra reial (Ophiophaga Hannah, de Michael Allen Smith), llangardaix cuc de dues potes (Bipes biporus, de Marlin Harms) i camaleó de l’Índia (Chamaeleo zeylanicus, de Shantanu Kuveskar).
ARCHOSAURIA: ANTICS REIS
Els arcosaures (literalment “rèptils dominants”) van ser el grup d’animals terrestres dominants durant el Mesozoic. Aquests van conquistar tots els habitats possibles fins a l’extinció de la majoria de grups a finals del Cretàcic. Alguns dels grups que es van extingir són els pseudosuquis (parents dels cocodrils actuals, ordre Crocodylia), els pterosaures (grans rèptils voladors) i els dinosaures (excepte els ocells actuals, clade Aves).
Dibuix del crani del dinosaure Massospondylus en el que es veuen les diferents obertures que caracteritzen als arcosaures diàpsids. Imatge de Steveoc 86.
Com podeu veure, els dos grups d’arcosaures actuals no podrien ser més diferents. Tanmateix, els cocodrils i les aus comparteixen un avantpassat comú, i estan més emparentats entre ells que amb la resta de rèptils.
Foto de dues espècies d’arcosaures actuals; un cocodril del Nil (Crocodylus niloticus) i un tàntal africà (Mycteria ibis). Foto de Tom Tarrant.
I LES TORTUGUES?
Les tortugues (ordre Testudines) sempre han estat un grup difícil de classificar. Les tortugues són els únics amniotes actuals que presenten un crani anàpsid, sense cap obertura post-ocular. Per això antigament, se les havia classificat com a descendents d’amniotes primitius (clade Anapsida, actualment en desús) o com a sauròpsids anàpsids primitius (dins del clade Parareptilia).
Esquelet de la tortuga extingida Meiolania platyceps que visqué a Nova Caledònia fins fa 3000 anys. En aquesta foto s’aprecia el crani compacte i sense obertures temporals. Foto de Fanny Schertzer.
Estudis moleculars recents, han desvelat que les tortugues són realment diàpsids que van perdre les obertures temporals secundàriament. El que encara divideix a la comunitat científica és si els testudinis están més emparentats amb els Lepidosauromorfs (lepidosaures i els seus avantpassats) o amb els Arcosauromorfs (arcosaures i els seus avantpassats).
Exemplar de tortuga lleopard (Stigmochelys pardalis) de Tanzània. Foto de Charles J. Sharp.
Com heu pogut veure, l’evolució dels amniotes és un tema molt complex. Esperem que amb aquesta entrada hagi quedat clar que:
- Els mamífers (sinàpsids) provenen d’un llinatge evolutiu diferent al dels rèptils (sauròpsids).
- Els sauròpsids inclouen als “rèptils” tradicionals (lepidosaures, arcosaures i tortugues) i a les aus (dins dels arcosaures).
- Encara queda molt per investigar sobre la posición de les tortugues (testudinis) dins l’arbre evolutiu dels sauròpsids.
Esquema modificat sobre les relacions evolutives entre els diferents grups d’amniotes.
REFERÈNCIES
Per a l’elaboració d’aquesta entrada s’han utilitzat les següents fonts:
- Imatge de portada de Henri Pidoux.
- Halliday & Adler (2007). La gran enciclopedia de los Anfibios y Reptiles. Editorial Libsa.
- Hickman, Roberts, Keen, Larson, l’Anson & Eisenhour (2009). Principios integrales de Zoología (decimocuarta edición). Mc Graw Hill.
- http://www.biologyreference.com/A-Ar/Amniote-Egg.html
- http://www.ucmp.berkeley.edu/vertebrates/tetrapods/amniota.html
- http://tolweb.org/Amniota
- http://onlinelibrary.wiley.com/doi/10.1111/j.1095-8312.1979.tb00027.x/abstract
- https://courses.candelalearning.com/osbiosec/chapter/29-4-reptiles/






 Imatge de
Imatge de  Foto d'un ratolí espinós del Caire (Acomys cahirinus), un mamífer que és capaç de desprendre's de la seva cua i regenerar-la. Foto de
Foto d'un ratolí espinós del Caire (Acomys cahirinus), un mamífer que és capaç de desprendre's de la seva cua i regenerar-la. Foto de 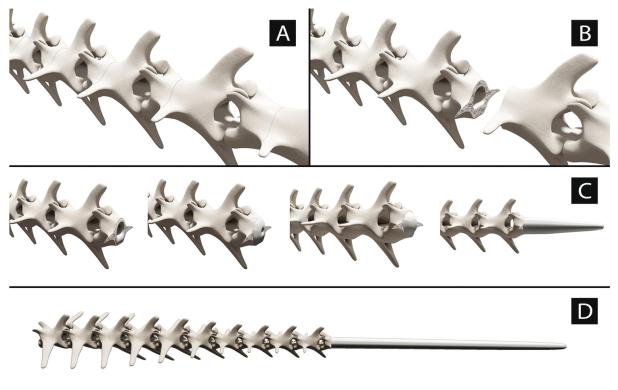 Model tridimensional de els plans de fractura de la cua d'un llangardaix i la regeneració post-autotomia d'un tub cartilaginós. Imatge extreta de
Model tridimensional de els plans de fractura de la cua d'un llangardaix i la regeneració post-autotomia d'un tub cartilaginós. Imatge extreta de  Foto d'una sargantana iberoprovençal (Podarcis liolepis) que ha perdut la cua. Foto de
Foto d'una sargantana iberoprovençal (Podarcis liolepis) que ha perdut la cua. Foto de  Detall de la cua d'un dragó comú (Tarentola mauritanica) que ha regenerat la cua sense acabar de perdre la cua original. Foto de
Detall de la cua d'un dragó comú (Tarentola mauritanica) que ha regenerat la cua sense acabar de perdre la cua original. Foto de  Capgròs de granota de bosc (Rana sylvatica) que, com en tots els amfibis, posposa el desenvolupament de les extremitats fins al moment de la metamorfosi. Foto de
Capgròs de granota de bosc (Rana sylvatica) que, com en tots els amfibis, posposa el desenvolupament de les extremitats fins al moment de la metamorfosi. Foto de  Esquema de la formació del blastema en el peix zebra (Danio rerio) un altre organisme model. Imatge de
Esquema de la formació del blastema en el peix zebra (Danio rerio) un altre organisme model. Imatge de  Foto d'un axolot, per
Foto d'un axolot, per 



















